
7、三元回收处理工艺流程
7.1、工艺流程图
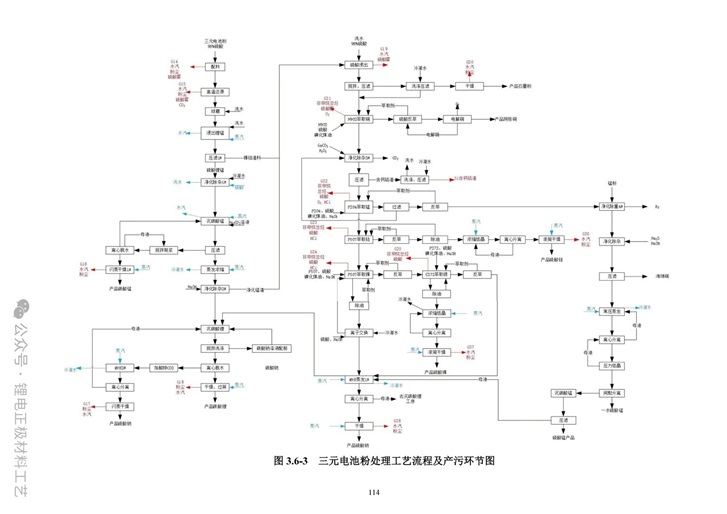
7.2、工艺流程说明
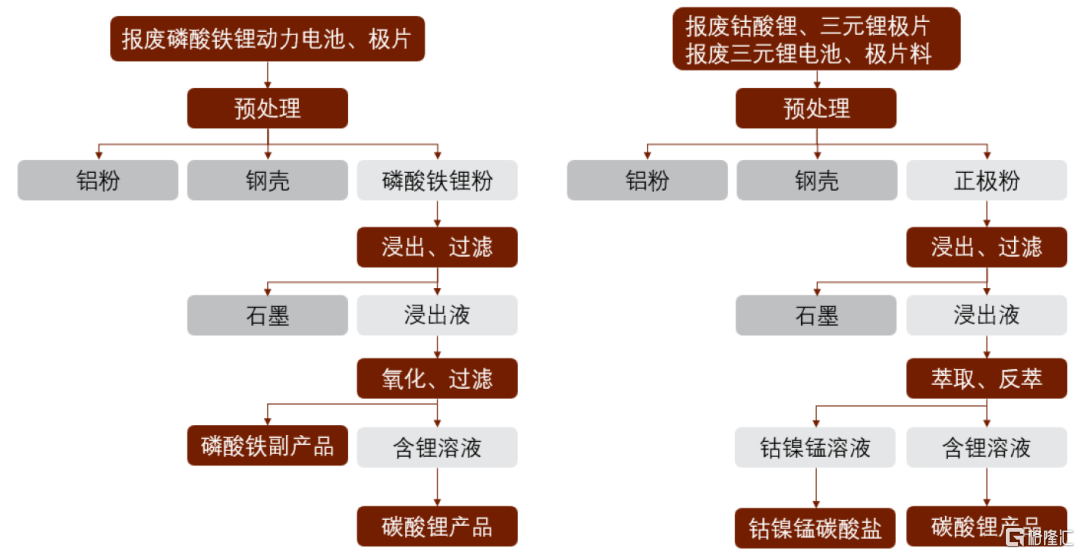
1)配料及高温还原:外购的含锂原料进入配料机,加入硫酸进行搅拌混合,待反 应完全后生成块状物料,后注入高温还原炉(电加热,加热温度约600~700℃,此温度 下硫酸不分解)进行还原反应,反应生成硫酸锂、硫酸锰、镍和钴的金属氧化物及硫酸 盐。(注:①硫酸加入量根据工艺需要,按锰浸出50%进行配比,锂浸出率100%配比;②硫酸与含锂原料在高温下反应60钟,99%硫酸被反应,未反应硫酸进入烟气中不在 反应固体中残留,即浸出后锂锰溶液呈中性)。
2)球磨、浸出锂锰、压滤:还原的固体物料经球磨机湿磨后,按固液比1:2加入 洗涤水(初始加冷凝水),浸出30-120分钟,浸出温度30~90℃。浸出液pH6~7。使用 压滤机固液分离出硫酸锂锰溶液和镍钴粉料。硫酸锂锰溶液进入净化除除工序,镍钴粉 料经洗涤后进入硫酸浸出工序,洗水返球磨工序作为补水。 Li₂SO₄(S)=Li₂SO₄(aq) MnSO₄(S)=MnSO₄(aq)
3)净化除杂1#:该工艺为技改调整工艺段。硫酸锂锰溶液在PH6-7的条件下通过 螯合树脂,螯合树脂对镍钴有优先吸附功能,其顺序为Ni>Co>Mn>>Li,其分配比 NI/Mn>10000,Co/Mn>1000,即当吸附后溶液中Mn含量为50g/l时,溶液中镍<0.005g/l, Co<0.05g/l,后续沉沉淀的碳酸锰产品质量能适用于电池级硫酸锰生产。吸附在树脂上 的镍钴用2mol的硫酸解吸得硫酸镍钴溶液,进入硫酸镍钴浸出系统回收镍钴即可,解吸后树脂用冷凝水清洗到pH=2即可进入再次吸附流程。
*反应方程式:
R-H+Ni²+=R2-Ni+H+吸附反应(PH大于1具有吸附能力)
R2-Ni+H+=R-H+Ni²+解吸反应(H+大于1mol具有解咐能力)
R-H+Co²+=R2-Co+H+吸附反应(PH大于1具有吸附能力)
R2-Co+H+=R-H+Co²+解吸反应(H+大于1mol具有解咐能力)。
4)沉淀碳酸锰:硫酸锂锰溶液加入碳酸钠,将锰以碳酸锰形式沉淀下来 Na₂CO₃+MnSO₄=MnCO₃J+Na₂SO₄
(1)压滤、洗涤、离心脱水:溶液与碳酸锰沉淀固液分离。硫酸锂溶液进入下一 工序,碳酸锰沉淀经压滤机内洗涤和离心分离后得含水5%碳酸锰,离心分离产生的母 液返回搅拌工序。
(2)闪蒸干燥:碳酸锰产品经闪蒸干燥后,得碳酸锰产品。
(3)蒸发浓缩:压滤3#后得10~15g/L硫酸锂溶液,再浓缩到25g/L,浓缩后液去 沉锂工段。
5)净化除杂2#:硫酸锂锰溶液重加入氢氧化钠(NaOH),去除溶液中的锰杂质;此工序产生净化锰渣,此沉淀物进入硫酸浸出工序进行生产。 NaOH+Mn²+=Mn(OH)₂J+2Na+
6)沉碳酸锂:将净化除重2#后所得硫酸锂溶液加氢氧化钠调碱度5g/L,然后加入 EDTA作为耦合剂,硫酸锂溶液中加入硫酸调节pH至6~8,调回pH6~8进入碳酸锂沉 淀工序。硫酸锂溶液中加入碳酸钠,通入蒸汽间接加热,控制其温度条件,生成碳酸锂沉淀。
MSO₄+NaOH=M (OH)₂J+Na₂SO₄
NaOH+H₂SO₄=Na₂SO₄+H₂O
Na₂CO₃+Li₂SO₄=Li₂CO₃J+Na₂SO₄
(1)离心分离:将碳酸锂与硫酸钠溶液分离,其中碳酸锂进入离心洗涤2#、干燥 工序,剩余硫酸钠溶液(母液)经加酸排CO₂工序后进入MVR蒸发工序。
(2)加酸排CO₂:碳酸钠溶液中加入H₂SO4排出CO₂,以除溶液中的CO₃2-。
(3)MVR2#蒸发:因沉碳酸锂时加入过量Na₂CO₃,此处加入H₂SO4将过量Na₂CO₃ 反应排出CO₂,排CO₂后硫酸钠溶液进入MVR蒸发工序,浓缩至母液中锂含量为10g/L 时进行离心分离3#,离心分离后浓度较高溶液进入闪蒸干燥2#工序得到产品硫酸钠结 晶(Na₂SO₄),剩余浓度较低母液返回沉淀碳酸锂。
(4)离心洗涤、干燥:碳酸锂使用冷凝水进行洗涤,洗涤后物料经干燥过筛,较 小颗粒直接作为产品碳酸锂(Li₂CO₃),筛上较大颗粒碳酸锂返回沉碳酸锂工序。洗涤 尾水返回配碳酸钠。
7)硫酸浸出、搅拌、压滤:将洗涤后得到的镍钴粉料按比例加入水浆化后进入硫 酸浸出工序,得到硫酸镍钴溶液。浸出后溶液进入搅拌槽进行搅拌增加硫酸与镍钴锰粉 料接触面积,使其反应更加充分,搅拌后溶液进入压滤机将硫酸镍、钴、锰溶液与渣料 固液分离,硫酸镍、钴、锰溶液进入N902萃取铜。渣料洗涤后再次压滤,其中洗水回 用于硫酸浸出镍钴工序,渣料进入干燥工序,干燥完成后得到产品石墨粉;H₂SO₄+MO=MSO₄+H₂O (M主要包含:Co²+、Ni²+、Mn²+、Cu²+、AI³+、Fe³+、Mg²+、Li+)
8)N902萃取铜、电解铜:
(1)N902萃取:硫酸镍钴溶液泵至N902萃取槽,萃取剂N902萃取槽,萃取剂N902中的H+与硫酸镍 钴溶液中的Cu²+进行置换,成为含铜负载有机相,再加入1N硫酸将有机相中钠离子等 反应出来,萃余液进入下一工序。
(2)硫酸反萃:含铜负载有机相通过与4N硫酸进行反萃,生成硫酸铜,萃取剂返回N902萃取铜工序。
(3)电解铜:经过反萃得到的硫酸铜溶液通过电解使铜在阴极富集,电解液(硫 酸溶液)返回反萃工序。
N902萃取:2(R'O)₂POOH+CuSO4=((R'O)₂PO0)₂Cu+H₂SO₄ (1)
N902反萃取:((R'O)₂PO0)₂Cu+H₂SO₄=2(R'O)₂POOH+CuSO₄ (2)
硫酸铜电解:CuSO₄+H₂O=Cu+H₂SO₄+0.50₂↑(3)

|



