
1)钴酸锂
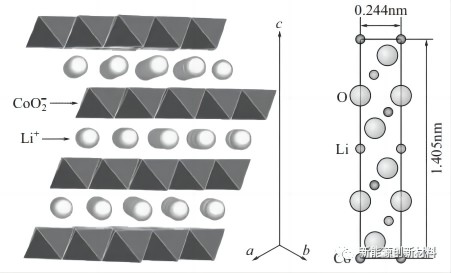
(1)钴酸锂 (LiCoO2 ) 为 α-NaFeO2 型层状结构, 属六方晶系,R3m 空间群, 6c 位上的 O2- 按 ABC 叠层立方堆积排列, 3a 位的 Li+ 和3b 位的Co3+ 分别交替占据 O2- 八面体孔隙, 呈层状排列。
(2)LiCoO2 中的 Co 为+3 价, 而在充电过程中会发生氧化反应变为+4 价, 从而脱出电子, 所发生的电化学反应可用下式表示:钴酸锂外观呈灰黑色粉体, 理论比容量为273mA・ h/g, 实际比容量通常为140~150mA・ h/g, 具有电压高、放电平稳、充填密度高、循环性好和适合大电流放电等优点
(3)并且 LiCoO2 的生产工艺简单, 较易合成性能稳定的产品。由于钴酸锂具有高的质量比能量, 目前主要用于小型高能量电池, 如手机和笔记本等3C数码领域。但其抗过充、高温安全性能不好。此外, Co资源稀缺, 成本高, 且有一定毒性。
2)三元材料
(1).三元材料LiCoxMnyNi1-x-yO2(简称 NCM) 与LiCoO2类似,同属α-NaFeO2型层状结构, 研究较多的体系主要有Li [Ni1/3Co1/3Mn1/3]O2、Li[Ni0.4Co0.2Mn0.4 ]O2 、 Li[Ni0.8Co0.1Mn0.1]O2和 Li[Ni0.5Co0.2Mn0.3]O2等。
(2).LiCoxMnyNi1-x-yO2三元材料中过渡金属离子的平均价态为+3 价, Co 以+3 价存在, Ni 以+2 价及+3 价存在, Mn 则以+4 价及+3 价存在, 其中+2 价的 Ni 和+4 价的 Mn 数量相等。充放电过程可用下式表示:这里以 LiCo1/3 Mn1/3Ni1/3 O2 的超结构模型为例讨论三元材料的可逆储锂机理。Li1-zCo1/3Mn1/3Ni1/3O2的充电脱锂过程分为3 个阶段:
① 0≤z ≤1/3 时对应的反应是将 Ni2+ 氧化成 Ni3+ ;
② 1/3≤z ≤2/3 时对应的反应是将 Ni3+ 氧化成 Ni4+ ;
③ 2/3≤z ≤1 时对应的反应是将 Co3+ 氧化成 Co4+ 。随着充电进行, 依次由 Ni2+/Ni3+ 、Ni3+/Ni4+ 和Co3+/Co4+ 电对的氧化,进行电荷补偿,主要通过 Ni2+/Ni3+ 和 Ni3+/Ni4+ 两个电对进行补偿, 而 Mn、Co两元素在充电过程中基本不发生变化, 氧化态分别稳定在+4 和+3 价;在充电后期则电子由氧原子提供。
(3).在LiCoxMnyNi1-x-yO2中, Ni 提供电化学所需要的电子, 有助于提高容量;但 Ni 含量增加会导致过渡金属离子混排趋势增加、循环性能恶化。Co能提高材料的导电性及倍率性能, 但过量 Co 会导致混排增大, 比容量也相应下降。Mn有利于改善安全性能, 但过量也会导致层状结构遭受破坏, 比容量降低, 循环稳定性变差。三元材料 NCM 综合了单一组分材料的优点, 具有明显的三元协同效应。三元材料基本物性和充放电平台与 LiCoO2 相近, 平均放电电压为3.6V 左右, 可逆比容量一般在150 ~180mA・ h/g。三元材料比 LiCoO2 容量高且成本低, 比LiNiO2 安全性好且易于合成,比LiMnO2更稳定且又拥有价格和环境友好优势。
(4)所以, 三元材料具有良好的市场前景, 目前主要用于小型锂离子电池和动力锂离子电池。典型的三元材料还有镍钴铝三元材料NCA (LiNi0.8Co0.15Al0.05O2 ) 。
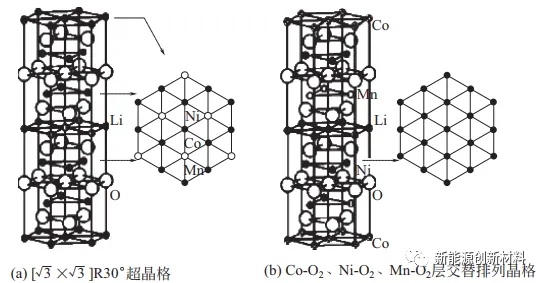
LiNi1/3Co1/3 Mn1/3O2 三元材料超结构示意图尖晶石型锰酸锂
3)尖晶石型锰酸锂 (LiMn2O4 ) 属于对称性立方晶系,单位晶格有32 个氧原子, 氧离子保持面心立方密堆积。LiMn2O4 中包含的3 价和4 价的 Mn 各占50%, 锰酸锂的电化学反应可用下式表示: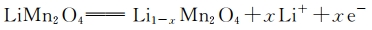 ;LiMn2O4 完全充电脱锂形成λ-MnO2 , 可能在化学计量不变的情况下发生相变, 经ε-MnO2 转变成没有活性的β-MnO2 , 导致容量衰减。 ;LiMn2O4 完全充电脱锂形成λ-MnO2 , 可能在化学计量不变的情况下发生相变, 经ε-MnO2 转变成没有活性的β-MnO2 , 导致容量衰减。
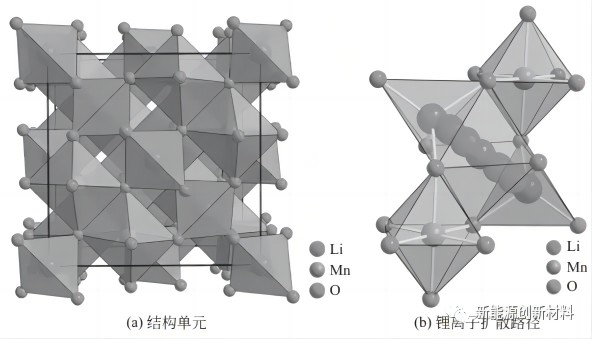
尖晶石型锰酸锂结构
(1)LiMn2O4 在充放电过程中, Mn 容易发生溶解。
(2)这是由于电解液中残留的微量水与含氟磷酸盐 (LiPF6 ) 反应生成 HF, 导致LiMn2O4中Mn3+发生歧化反应生成Mn4+和Mn2+, 其中Mn4+则形成 MnO2留在材料中, Mn2+ 进入电解液;
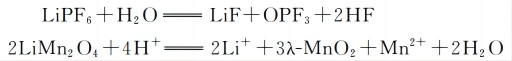
(3)进入电解液的 Mn2+ 还可以进一步反应生成 MnO 并沉积在负极上;从上述方程式上还可以看出, Mn3+ 的歧化反应过程会生成 H2O, 而 H2O 又会进一步促使 HF 的产生, 这便构成了一个恶性循环。这是一个自催化的反应, 而且温度的升高会加剧这一反应。因此尖晶石 LiMn2O4在高温下容量会快速衰减。尖晶石结构锰酸锂 (LiMn2O4) 优点是电压高、 抗过充性能好、安全性能好、容易制备, 同时 Mn 资源丰富、价格便宜、无毒无污染; 缺点是比容量低且可提升空间小, 在正常的充放电使用过程中 Mn 会在电解质中缓慢溶解, 深度充放电和高温条件下晶格畸变较为严重, 导致循环性能变差。目前LiMn2O4主要用于动力锂离子电池。

|



