(4)实验现象与实验结果的记录
A.过程中的有关数据记录:碳酸锰合成过程中的数据记录如表1所示:

B.二价锰含量的分析结果记录
a.G--样品质量;0.05494--每毫摩尔Mn之克数;碳酸锰含量测定数据及结果如表2所示.
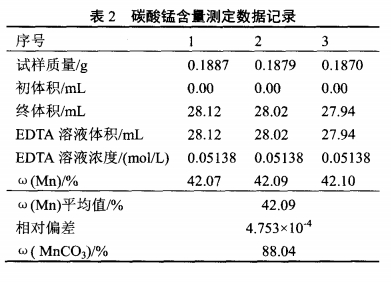
b.从表2可以看出,合成碳酸锰的纯度大于88%,远远超过了国标工业级碳酸锰 44%的标准(国标号:CAS#:598―62.9),可用作工业生产原料。
3)结果与讨论
(1)还原剂种类对碳酸锰产率的影响:实验过程中分别用锌粉、过氧化氢、铁粉、硫化亚铁为还原剂,反应起始物的质量为5g,判别还原剂对碳酸锰产量的影响,结果如表3所示

*从表3可以看出,使用硫化亚铁、过氧化氢做还原剂比锌粉、铁粉生成碳酸锰的量要多,但是使用硫化亚铁容易引进硫、铁等杂质,是后续过程不好处理,而且对环境造成二次污染,所以后续过程都使用过氧化氢做还原剂;
(2)过氧化氢用量对碳酸锰产率的影响:固定反应时间和反应温度,改变H2O2用量,结果如表4所示。

*从表4可以看出,还原剂H2O2用量增加,MnCO3生成量也随着增加,但是当H2O2用量增大到某一程度,MnCO3生成量又逐渐减小.这是因为过氧化氢用量过低,不能将二氧化锰中的四价锰完全转化为二价锰,所以碳酸锰的生成量较少,随着过氧化氢用量的增加MnCO3的产量有明显提高,但当H2O2增加到一定程度碳酸锰的产量反而下降,这可能是因为过量的H202反而将生成的Mn2+氧化导致碳酸锰产量下降。
(3)本文采用了人工分选与湿法相结合技术,回收废旧锌锰电池中的锰,采用条件为:用3O%过氧化氢为还原剂,硫酸介质,以饱和碳酸氢铵溶液为沉淀剂,结果得到了纯度较高的碳酸锰,回收率也比较高.而且该实验室回收方法简便易行,值得推广到实际工艺生产过程中。

|



